Fontos frissítés az orvostechnikai eszközök gazdasági szereplői számára - EUDAMED modulok: kötelező használat 2026. május 28-tól
Az Európai Bizottság hivatalosan is közzétette az European Commission döntését (EU 2025/2371), melynek értelmében az EUDAMED első négy modulja „teljesítette a funkcionális követelményeket” — erről a 2025. november 27-i számában megjelent az Official Journal of the European Union (OJEU).
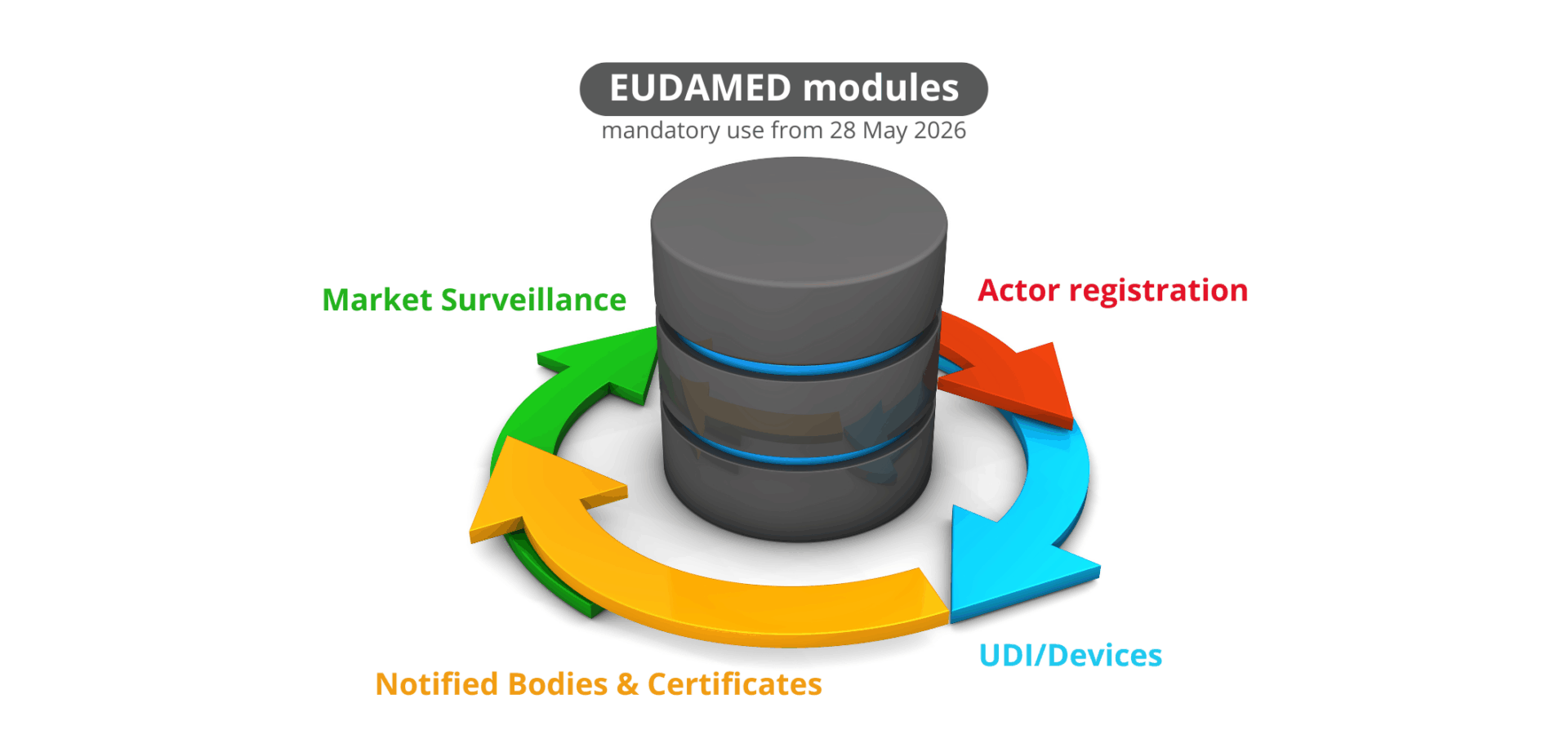
Mely modulok válnak kötelezővé?
A kötelező regisztrációs/publikációs modulok a következők:
- Gazdasági szereplők regisztrációja (Actor registration)
- UDI / Eszközregisztráció (UDI/Devices)
- Tanúsítványok, bejelentett szervezetek (Notified Bodies & Certificates)
- Piacfelügyelet (Market Surveillance)
Fontos határidők
- Az OJEU-ban megjelent értesítés 2025. november 27-én történt.
- Az EUDAMED első négy modulját 2026. május 28-tól kötelező használatba venni.
- Ez azt jelenti, hogy gyártók, forgalmazók, importőrök, meghatalmazott képviselők számára hat hónap áll rendelkezésre az adatok feltöltésére és regisztrációra.
Mit jelent mindez az Ön számára?
- Kötelező regisztráció: Minden gyártó, importőr, meghatalmazott képviselő — EU-székhelyű vagy kívüli — számára SRN azonosító kérvényezése az Actor-modulban.
- Eszköz- és UDI-regisztráció: Az összes forgalomba helyezett orvostechnikai eszközt és IVD-t regisztrálni kell az UDI/Devices modulban. Ez alól nem lesz kivétel 2026. május 28-át követően.
- Tanúsítványok és Notified Body adatok feltöltése: Az Ön tanúsítványainak, a bejelentett szervezet adatainak is meg kell jelenniük az adatbázisban.
- Piacfelügyelet és megfelelőség biztosítása: A modul lehetővé teszi az uniós szervek számára az eszközök követését és a piacfelügyeleti eljárások egyszerűsítését.
Mit tegyen most?
- Ellenőrizze, hogy cége regisztrált-e már az EUDAMED Actor-modulban, és ha nem — kérvényezze az SRN-t mihamarabb.
- Készítse elő az összes orvostechnikai eszköz dokumentációját (UDI, device-data, tanúsítványok), hogy 2026. május 28-ig feltölthetők legyenek.
- Ha EU-n kívüli gyártóként/importőrként működik, biztosítsa, hogy EU-képviselője (Authorized Representative) időben regisztráljon.
Összefoglalás
Az EUDAMED négy első moduljának kötelezővé tétele 2026. május 28-i hatállyal mérföldkő az orvostechnikai piac szabályozásában: a regisztráció, átláthatóság és piacfelügyelet új korszakába lépünk. Javasoljuk, hogy most azonnal indítsa el a felkészülést, hogy elkerülje a határidő lejárta előtti torlódásokat és a szabályozási kockázatokat.
Források:
https://health.ec.europa.eu/medical-devices-eudamed/getting-ready_en
Szerző: Tauberné Dr. Jakab Katalin, klinikai szakértő

